

“神农尝百草,一日而遇七十毒”,形象记录了中药起源于人类对各种新鲜药材(鲜药)的认识。晋代葛洪《肘后备急方》中“青蒿一握,水二升渍,捣绞汁,尽服之”,对于鲜药利用的记载,成为诺贝尔生理学或医学奖获得者屠呦呦发现青蒿素的思想理论源泉。鲜药未经加工,保持了天然状态,但对于鲜药的科学认识还极其有限。
人参(Panax ginseng C. A. Mey)为“百草之王”。味甘微寒,具大补元气,复脉固脱,补脾益肺,生津安神之功效,东西方都应用广泛。2019年11月27日,我院曹鹏研究员团队在肿瘤免疫治疗协会(SITC)官方杂志Journal for ImmunoTherapy of Cancer (免疫学1区, IF: 8.676) 在线发表论文“Ginseng-derived nanoparticles alter macrophage polarization to inhibit melanoma growth”, 该文首次报道了从新鲜人参中提取的囊泡通过极化巨噬细胞,抑制黑色素肿瘤的生长。本文的通讯作者为曹鹏研究员,第一作者为曹萌副研究员,助理研究员颜怀江和博士研究生韩暄等人参与了研究工作。
细胞外囊泡(extracellular vesicles,EVs)是由细胞分泌的纳米尺寸的脂质膜封闭结构。EVs作为细胞间通讯的重要介质,影响生理和病理状况。鉴于其转移生物活性成分和克服生物屏障的能力,EVs越来越多地被探索为潜在的治疗剂。目前对于细胞外囊泡的研究,主要集中在哺乳动物细胞上清液和体液,而植物,特别是药用植物囊泡领域的研究十分有限。
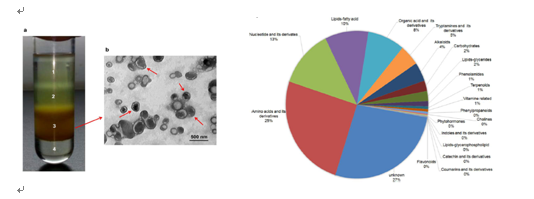
曹鹏研究团队从2016年开始开展了中药鲜药的研究,发现从新鲜人参的汁液中可以提取到类似于动物细胞分泌的胞外囊泡,并将这种囊泡命名为Ginseng-derived nanoparticles(GDNPs)。研究人员发现这种人参来源的植物囊泡的直径为300 nm左右。多组学分析显示,GDNPs富含多种人参来源的蛋白、脂类、核酸和小分子。
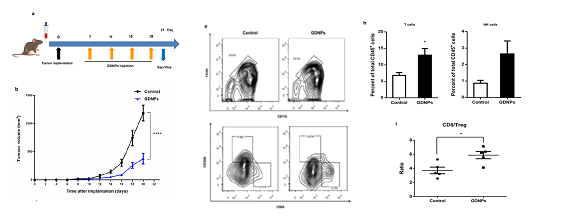
研究发现GDNPs对单核-巨噬细胞有着很强的亲嗜性,能够被巨噬细胞有效地吞噬,同时促进巨噬细胞向具有抗肿瘤作用的M1型巨噬细胞极化,并且极化的巨噬细胞分泌大量ROS杀伤肿瘤。经过进一步的分析,证实GDNPs极化巨噬细胞的主要机制是通过其含有的神经酰胺(Ceramide)活化巨噬细胞表面的Toll样受体4(TLR4)。荷瘤小鼠实验结果表明GDNPs的治疗有效促进肿瘤微环境中的肿瘤相关巨噬细胞(tumor associated macrophage,TAM)向抗肿瘤的M1型巨噬细胞极化,解除肿瘤微环境免疫抑制状态,活化CD8+T淋巴细胞和NK细胞,抑制黑色素瘤的生长。
该研究首次发现囊泡是鲜药人参发挥药效的重要物质基础,加深了对中药的科学认识,为拓展鲜药利用途径带来新的启示; 同时也是首次发现药用植物来源的囊泡具有重编程肿瘤相关巨噬细胞的功能,GDNPs对于肿瘤的免疫治疗可能带来新的希望。
原文链接:
https://jitc.biomedcentral.com/articles/10.1186/s40425-019-0817-4